植物总RNA提取试剂盒品牌:genefist | 货号:TR02 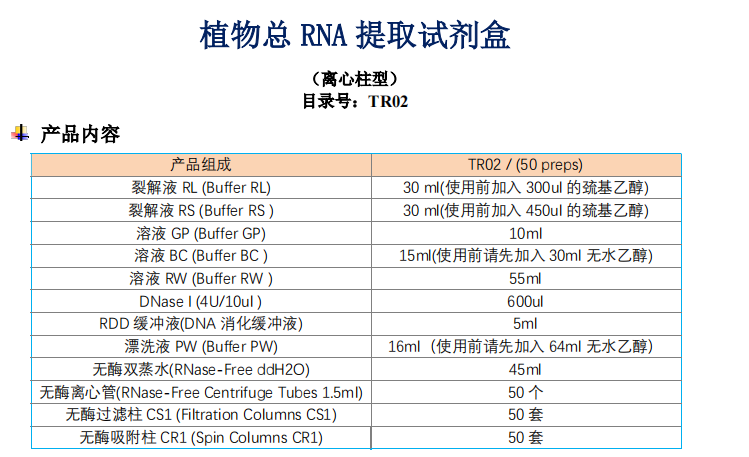
储存条件
“裂解液RS” 和 “DNase I(DNase I 冻干粉溶解于专用保存液)”,储存于-20℃。其他试剂室温(15-25℃)保存。
产品简介
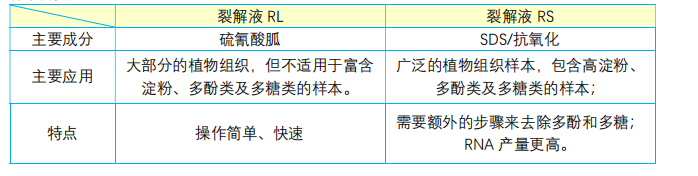
由于植物的细胞结构和代谢活性在物种、组织类型和发育阶段之间可能存在显著差异,因此没有一种通用的裂解溶液或独特的方法可以同样适用于所有植物样品。本试剂盒包含两种可供选择的裂解缓冲液系统:裂解缓冲液 RL(含硫氰酸胍)和裂解缓冲液 RS(含 SDS/抗氧化剂),适用于各种植物和真菌样品。“裂解液RL”含硫氰酸胍,此提取方案适用于大部分的植物组织,操作简单快速,但它不适用于富含淀粉、多酚类及多糖类的样本,因为裂解液RL加入上述样本后,会使样本变非常粘稠甚至凝固。
“裂解液RS”,采用我司独特的“SDS/抗氧化”的方式,可适用于广泛的植物组织,包含草本植物与本本植物的叶片、具高粘性的多糖多酚类及种子胚乳的植物样本,此提取方案,增加了额外步骤去除多酚和多糖,RNA的提取总量更高。
本试剂盒提取的总 RNA 纯度高,基本没有基因组、蛋白和其它杂质的污染,可用于 PCR、Blot、分子克隆等多种下游实验。
预防RNase污染,应注意以下几方面
1.经常更换新手套,因为皮肤经常带有细菌,可能导致RNase污染。
2.使用无RNase的塑料制品和枪头避免交叉污染。
3.RNA在裂解液RL中时不会被RNase降解。但提取后继续处理过程中应使用不含RNase的塑料和玻璃器皿。玻璃器皿可在150℃烘烤4 h,塑料器皿可在0.5 M NaOH中浸泡10 min,然后用水彻底清洗,再灭菌,即可去除RNase。
4.配制溶液应使用无RNase的水(将水加入到干净的玻璃瓶中,加入DEPC至终浓度0.1%(V/V),高压灭菌)。
使用前注意事项
1.裂解液 RL:使用前请添加 300ul 巯基乙醇,添加过巯基乙醇的裂解液 4℃保存。
2.裂解液 RS:使用前请于 50℃水浴将裂解液完全回溶,并添加 450ul 巯基乙醇;添加过巯基乙醇的裂解液RS 继续保存于-20℃(建议将添加过巯基乙醇的裂解液 RS 于无酶管分装成小量,再保存于-20℃)。
3.溶液 BC:使用前请添加 30ml 无水乙醇。
4.漂洗液 PW:使用前请向添加 64ml 无水乙醇。
5.为确保 RNA 的品质及产量,应尽量收取新鲜的动物组织进行 RNA 提取,或将组织立即以液氮冷冻,储存于-70℃,组织亦可保存在 RANstore 样本保存液(目录号:TR38)中。
6.凤梨和兰花推荐采用“裂解液 RL”。
操作步骤
一、裂解液 RL 操作步骤:
1.匀浆处理
50-100 mg 植物叶片在液氮中迅速研磨成粉末,加入 450ul RL(使用前请先检查是否已加入 β-巯基乙醇),涡旋剧烈震荡混匀,并于 56℃孵育 3 分钟。
注意 1:在 56℃孵育 1-3 min 将有助于植物组织裂解,但是对于某些富含淀粉的样品,请不要加热处理,防止因淀粉引起的样品膨胀现象。
注意 2:由于植物多样性非常丰富,而且同种植物的不同生长发育阶段和不同组织的 RNA 含量都不相同,请根据具体实验情况选择合适的植物材料的用量。
2.将所有溶液转移至过滤柱 CS1 上(过滤柱 CS1 放在收集管中),12,000 rpm(~13,400×g)离心 2-5 min,小心吸取收集管中的上清至 RNase-Free 的离心管中,吸头尽量避免接触收集管中的细胞碎片沉淀。
注意:由于裂解液较粘稠,所以将溶液转移至过滤柱时,可以剪去部分吸头末端。
3.缓慢加入 0.5 倍上清体积的无水乙醇,混匀(此时可能会出现沉淀),转至“RNA 提取”步骤。
4.将所得“裂解液/乙醇混合液”(含沉淀),移取至吸附柱 CR1 中(吸附柱 CR1 放入收集管中),12,000 rpm(~13,400×g )离心 30-60 sec,倒掉收集管中的废液,将吸附柱 CR1 放回收集管中。
注意:将溶液和沉淀转移至吸附柱 CR1 时,如果体积大于吸附柱容量,可以分次完成。
5.向吸附柱 CR1 中加入 500ul 溶液 RW,12,000 rpm (~13,400×g )离心离心 1 min,丢弃滤液,将吸附柱CR1 放回收集管中。
6.DNase Ⅰ降解。
每一纯化反应,请将 80 ul DNase 消化液与 10ul DNaseⅠ预先混合在新的离心管(轻弹或翻转离心管以混合均匀,请勿震荡),将 90 ul “DNaseⅠ工作液”加入至吸附柱的膜中心,于室温(25~28℃)孵育15 分钟。
注意:如同时操作多组样本,请使用前现配新鲜的 DNaseⅠ工作液,请勿预先配制保存 DNaseⅠ工作液。
7.向吸附柱 CR1 中加入 500μl 溶液 RW,12,000 rpm(~13,400×g)离心 1 min,倒掉收集管中的废液,将吸附柱 CR1 放回收集管中。
8.向吸附柱 CR1 中加入 600μl 漂洗液 PW(使用前请先检查是否已加入乙醇),12,000 rpm(~13,400×g) 离心 1 min,倒掉收集管中的废液,将吸附柱 CR1 放回收集管中。
9.重复操作步骤 8。
10.12,000 rpm(~13,400×g)离心 3 min,将吸附柱 CR1 置于室温放置数分钟,以彻底晾干吸附材料中残余
的乙醇。
注意:此步骤目的是将吸附柱中残余的漂洗液去除,离心后将吸附柱 CR1 在室温放置片刻,以充分晾干。如果有漂洗液残留,可能会影响后续的 RT 等实验。
11.将吸附柱 CR1 转入一个新的 RNase-Free 离心管中,加入 30-100 μl 无酶双蒸水至吸附柱的膜中心,室温静置 2 min,12,000 rpm(~13,400×g)离心 1 min,得到 RNA 溶液。
注意:洗脱缓冲液体积不应少于 30 μl,体积过小影响回收效率;RNA 溶液请于-70℃保存。
二、裂解液 RS 操作步骤
1.匀浆处理:50-100 mg 植物叶片在液氮中迅速研磨成粉末,加入 450 μl 裂解液 RS(使用前请先检查是否已加入 β-巯基乙醇),立即涡旋剧烈震荡混匀,并于 56℃孵育 5-10 分钟,每隔一段时间可翻转混合离心管。
注意:由于植物多样性非常丰富,而且同种植物的不同生长发育阶段和不同组织的 RNA 含量都不相同,请根据具体实验情况选择合适的植物材料的用量。
2.加入 150ul 的溶液 GP 至裂解液中,混合均匀,于冰上孵育 5 分钟,12,000rpm(~13,400×g)离心 5 min。
注意:溶液会呈现雾状,为界面活性剂、蛋白质、多糖及二次代谢物的沉淀物。
3.移取上清液至过滤柱 CS1 上(过滤柱 CS1 放在收集管中),12,000 rpm(~13,400×g)离心 2 min。
4.小心吸取收集管中的上清至新的 RNase-Free 离心管中,吸头尽量避免接触收集管中的细胞碎片沉淀。
5.向溶液中加入 1.5 倍体积的溶液 BC(已添加无水乙醇),以震荡或移液器吸吐混合均匀。
注意:加入溶液 BC 后会形成丝状沉淀物,不影响 RNA 提取。
6.移取混合液(连同沉淀物一起)至吸附柱 CR1(吸附柱 CR1 放在收集管中),12,000 rpm(~13,400×g) 离心 1 min,丢弃滤液,将吸附柱 CR1 放回收集管中。
注意:如果混合液体积大于吸附柱容量,可以分次完成。
7.向吸附柱 CR1 中加入 500ul 溶液 RW,12,000rpm(~13,400×g)离心 1min,丢弃滤液,将吸附柱 CR1 放回收集管中。
8.DNase Ⅰ降解。
每一纯化反应,请将 80 ul DNase 消化液与 2ul DNaseⅠ预先混合在新的离心管(轻弹或翻转离心管以混合均匀,请勿震荡),将 82 ul “DNaseⅠ工作液”加入至吸附柱的膜中心,于室温(25~28℃)孵育15 分钟。
注意:如同时操作多组样本,请使用前现配新鲜的 DNaseⅠ工作液,请勿预先配制保存 DNaseⅠ工作液。
9.向吸附柱 CR1 中加入 500μl 溶液 RW,12,000 rpm(~13,400×g)离心 1 min,倒掉收集管中的废液,将吸附柱 CR1 放回收集管中。
10.向吸附柱 CR1 中加入 600 μl 漂洗液 PW(使用前请先检查是否已加入乙醇),12,000 rpm(~13,400×g)离心 1 min,丢弃滤液,将吸附柱 CR1 放回收集管中。
11.重复操作步骤 10。
12.12,000rpm(~13,400×g)离心 3 min,将吸附柱 CR1 置于室温放置数分钟,以彻底晾干吸附柱中残余的乙醇。
注意:此步骤目的是将吸附柱中残余的漂洗液去除,离心后将吸附柱 CR1 在室温放置片刻,以充分晾干。
如果有漂洗液残留,可能会影响后续的 RT 等实验。
13.将吸附柱 CR1 转入一个新的 RNase-Free 离心管中,加入 30-100 μl 无酶双蒸水至吸附柱的膜中心,室
温静置 2 min,12,000 rpm(~13,400×g)离心 1 min,得到 RNA 溶液。
注意:洗脱液体积不应少于 30μl,体积过小影响回收效率。为了增加产量,可将步骤 13 得到的 RNA 溶液再加入吸附柱 CR1,放置 2min,12,000rpm(~13,400×g)离心 1min,得到 RNA 溶液。RNA 溶液-70℃中保存。
附录:从高度黏稠性的富含多酚及多糖成分的样本中提取 RNA
樟科植物样本,在裂解后粘稠度高、移取困难,可直接于过滤柱中进行裂解,以减少移液器吸取的步骤。
1.将过滤柱 CS1 于冰上预冷,秤取不超过 30mg 的样本组织,于液氮中迅速研磨,并将研磨的样本直接转移至预冷的过滤柱 CS1 里(过滤柱 CS1 放在收集管中)。
2.加入 600ul 裂解液 RS(已添加巯基乙醇)至过滤柱,于 60℃金属浴孵育 10 分钟。
3.12,000 rpm(~13,400×g)离心 5 min,将收集管中的滤液移取至新的 1.5ml 离心管,请避免吸取到沉淀物。
注意:有些样本可能会堵塞过滤柱,可再次离心,或将管柱中剩余的裂解液移至新的过滤柱 CS1 再次离
心。
4.加入 1/3 倍体积的溶液 GP 至滤液中,混合均匀,于冰上孵育 5 分钟,12,000 rpm(~13,400×g)离心离心 5 min,将上清液小心转移至新的 1.5ml 离心管,不要触碰或移取固体沉淀。转至上面“操作步骤5”。
上海金畔生物科技有限公司代理各种进口试剂耗材,欢迎来电咨询18301939375,量多优惠。网站可提供的所有产品和服务均不得用于人体或动物的临床诊断或治疗,仅可用于科研等非医疗目的。
